
时间:2023-12-31 点击数:
近日,我院陆军教授、张瑜教授课题组在细胞衰老领域取得新进展。课题组揭示了progerin/PTBP1/BUBR1轴介导儿童早衰症(HGPS)细胞衰老的全新机制。发现特异性progerin-C末端肽UPCP通过解除早老蛋白progerin与有丝分裂纺锤体组装检验点组分BUBR1之间的相互作用进而纠正BUBR1的错误定位,延缓HPGS早衰鼠衰老,为HGPS的治疗提供了新的思路(图1)。
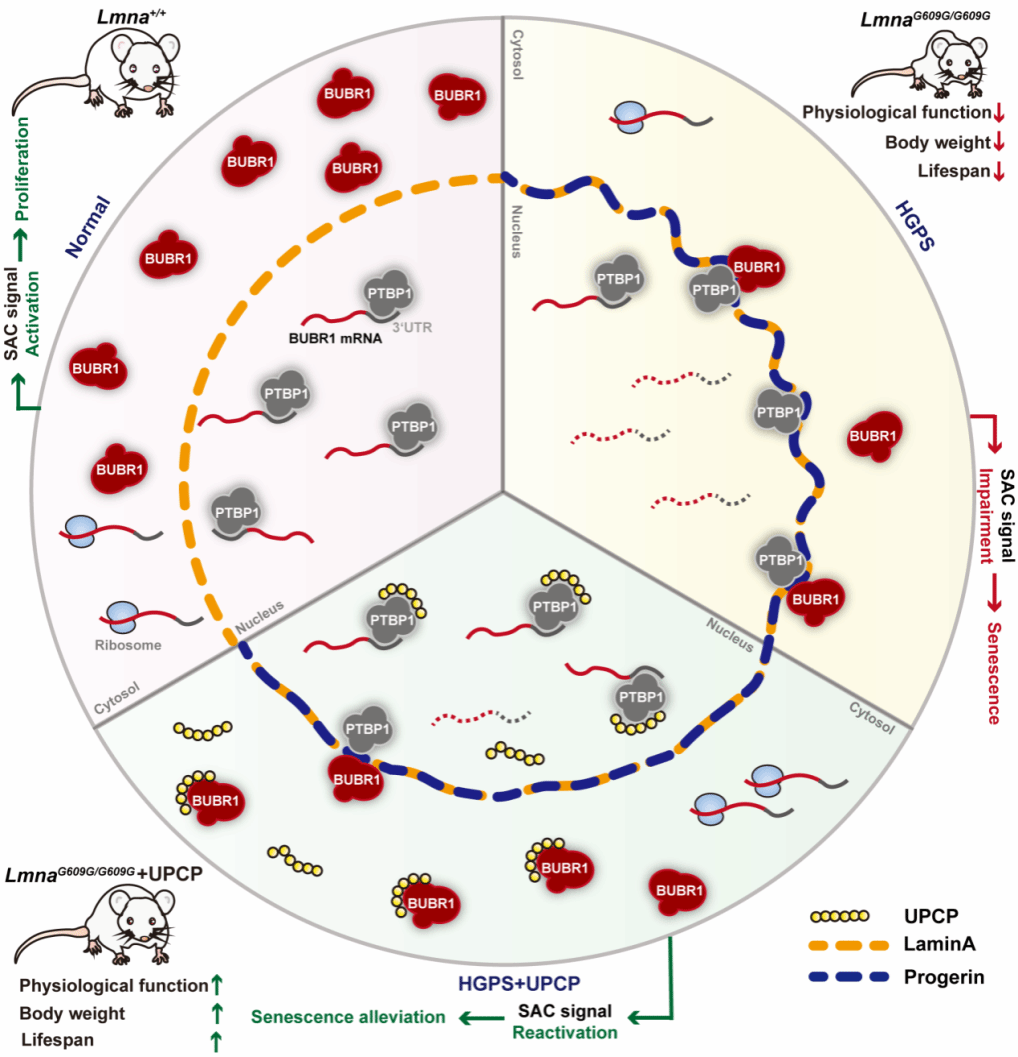
图1. 研究发现总结模型
相关研究成果以“Unique progerin C-terminal peptide ameliorates Hutchinson–Gilford progeria syndrome phenotype by rescuing BUBR1”为题发表于 Nature核心子刊之一Nature Aging(自然-衰老)。我院张娜博士和胡倩颖博士为共同第一作者。我院张瑜教授、陆军教授、吉林大学动物科学学院李占军教授为共同通讯作者。
该工作发表后随即被Nature期刊遴选为研究亮点(Research Highlight),以“Protein double act implicated in rapid ageing of children”为题进行了报道,从阐明儿童早衰症有丝分裂障碍的全新机制并提供新的儿童早衰症潜在治疗策略的角度,充分肯定了团队发表在Nature Aging研究工作的价值与意义(Nature 614,392,2023)。
Nature Aging期刊同期在“News & views”栏目配发题为 “Missing checkpoints in premature aging” 的长评论文章,认为该工作解释了儿童早衰症中令人困惑的有丝分裂表型(Nature Aging, 3, 146–147, 2023)。
哈钦森-吉尔福德儿童早衰综合征(Hutchinson-Gilford progeria syndrome, HGPS)是儿童早年衰老综合征中最典型、最常见的一种过早老化性致死疾病。HGPS 患者衰老速度是正常衰老速度的5~10倍,平均寿命仅14.6岁。HGPS细胞的衰老模式被认为是生理性衰老的加速版。因此,探究 HGPS 衰老的分子机制,不仅对于揭示 HGPS 的发病机理及开发新的治疗策略具有重要意义,同时对于理解正常人体衰老的分子机制也具有重要价值。治疗方面,目前仍缺乏有效的HGPS治疗手段,亟需开发新的HGPS治疗策略。肽类药物因其分子量小、毒性低等优势已被用于多种疾病的治疗,肽策略能否用于儿童早衰症的治疗尚不明确。本项研究工作提供的实验证据,为理解HGPS衰老过程中异常的有丝分裂表型具有重要的理论价值。团队开发并明确了progerin C-末端特异性肽UPCP治疗HGPS的可行性,为HGPS的治疗提供了新的肽策略。
课题组长期致力于衰老及衰老相关疾病的表观遗传机制方面的研究。前期工作系统揭示了多种蛋白质的精氨酸甲基化修饰及microRNA网络调控细胞衰老及衰老相关疾病的分子机制。近年来,相关标志性成果相继发表在EMBO Journal、Cell Death & Differentiation等期刊上,极大提升了我院在表观遗传和细胞衰老领域的学术影响力,积极促进了生物学学科的建设和发展。
相关链接:
Nature aging论文:https://doi.org/10.1038/s43587-023-00361-w
Nature期刊Research Highlight:https://www.nature.com/articles/d41586-023-00355-z
Nature aging期刊News & Views评论文章:https://www.nature.com/articles/s43587-022-00351-4
EMBO Journal 论文:https://www.embopress.org/doi/full/10.15252/embj.2022110937
Cell Death & Differentiation论文:https://www.nature.com/articles/s41418-020-0562-8